《细胞》:中国科学家开发阿尔茨海默病新疗法!
来源:学术经纬 2025-11-23 16:48
该研究发现了一个极具潜力的AD治疗靶点——胆囊收缩素B受体(CCKBR)。此外,研究团队设计出一种能够精准靶向该受体、高效穿透血脑屏障的潜在药物分子3r1。
阿尔茨海默病(AD)是一种严重的神经退行性疾病,患者会经历记忆和认知功能衰退,甚至丧失自理能力。多年来,科学家一直在寻找能够有效延缓甚至逆转其病程的药物。然而,由于病因复杂、血脑屏障难以穿透、药物靶点不明确等挑战,至今仍缺乏根本性治疗方法。
今日,北京大学/山东大学孙金鹏教授与香港城市大学贺菊芳教授,北京大学张勇教授,铁璐副教授,香港中文大学(深圳)杜洋教授,北京宣武医院唐毅主任通力合作在《细胞》杂志发表了全新论文。该研究发现了一个极具潜力的AD治疗靶点——胆囊收缩素B受体(CCKBR)。此外,研究团队设计出一种能够精准靶向该受体、高效穿透血脑屏障的潜在药物分子3r1。动物实验显示,3r1可以抑制神经/突触损伤,清除Aβ沉积,为AD的精准治疗提供了新策略。

内嗅皮层是信息从大脑皮层传递到海马的“中转站”,也是记忆形成与提取的关键枢纽。这个区域中大量存在一种叫做胆囊收缩素的神经肽,而它的受体——CCKBR,就像是一个“信号接收站”,在学习和记忆中扮演着至关重要的角色。小鼠缺乏CCKBR时,在迷宫测试中的表现会格外差,记忆力下降明显。
此外,CCKBR被激活后的下游信号通路包括Gs、Gi和Gq三条通路。研究团队发现重度痴呆患者的脑脊液多肽成分对CCKBR的Gq信号激活能力显著低于轻度痴呆患者,对Gi信号的激活能力高于轻度痴呆患者。这说明CCKBR的Gq信号活力随着AD病程的加重而逐渐减弱,而Gi信号活力则相反。
为了更好地理解CCKBR的作用机制,作者借助冷冻电镜技术,首次解析了CCKBR被CCK8激活后的三维结构。结果显示,CCKBR的活性口袋会分为三个功能区,可以分别与三个G蛋白(Gs、Gq、Gi)结合。
并且当不同的G蛋白结合时,会诱导受体发生不同的构象变化,从而“偏好性”地激活对应的某一条下游通路。这也解释了为什么激活同一个CCKBR受体,可能会产生不同的生理效应。
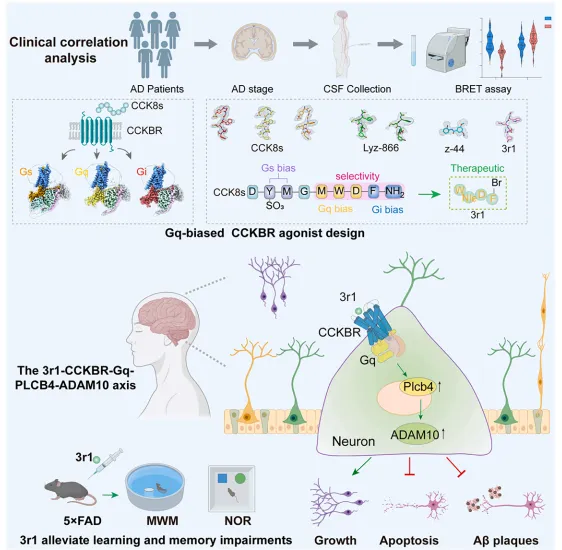
▲研究示意图(图片来源:参考资料[1])
后续的测试中,研究者发现CCKBR下游Gs或Gq信号通路的激活能介导神经保护作用,而Gi通路则不介导这一过程,这提示CCKBR下游Gs或Gq信号通路参与调控神经元损伤修复。
为了实现对这些信号通路的人为调控,研究团队设计了不同的激动剂。其中表现最为亮眼的是能激活Gq信号通路的激动剂3r1。相较于内源性配体CCK8s,3r1具备良好的血脑屏障穿透性和更长的半衰期。
在AD小鼠模型中,3r1治疗能显著改善小鼠的空间学习与记忆能力,并促进海马长时程增强(LTP),减少Aβ斑块沉积和Tau蛋白磷酸化。这一发现提示,靶向CCKBR的Gq偏好性激动剂3r1在改善AD相关认知缺陷方面具有治疗效果。
另外,研究团队还进一步找到了3r1激活的关键下游分子,包括磷脂酶Cβ4(PLCB4)和ADAM10。综上,该研究首次阐明了CCKBR偏向性信号在AD治疗中的潜力。所开发的Gq偏向性激动剂3r1具有更好的药代动力学特性,为AD的精准治疗提供了新方向。
参考资料:
[1] Elucidating pathway-selective biased CCKBR agonism for Alzheimer’s disease treatment. Cell (2025). DOI: 10.1016/j.cell.2025.10.034
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


